
和黄医药2021年主要财务数据
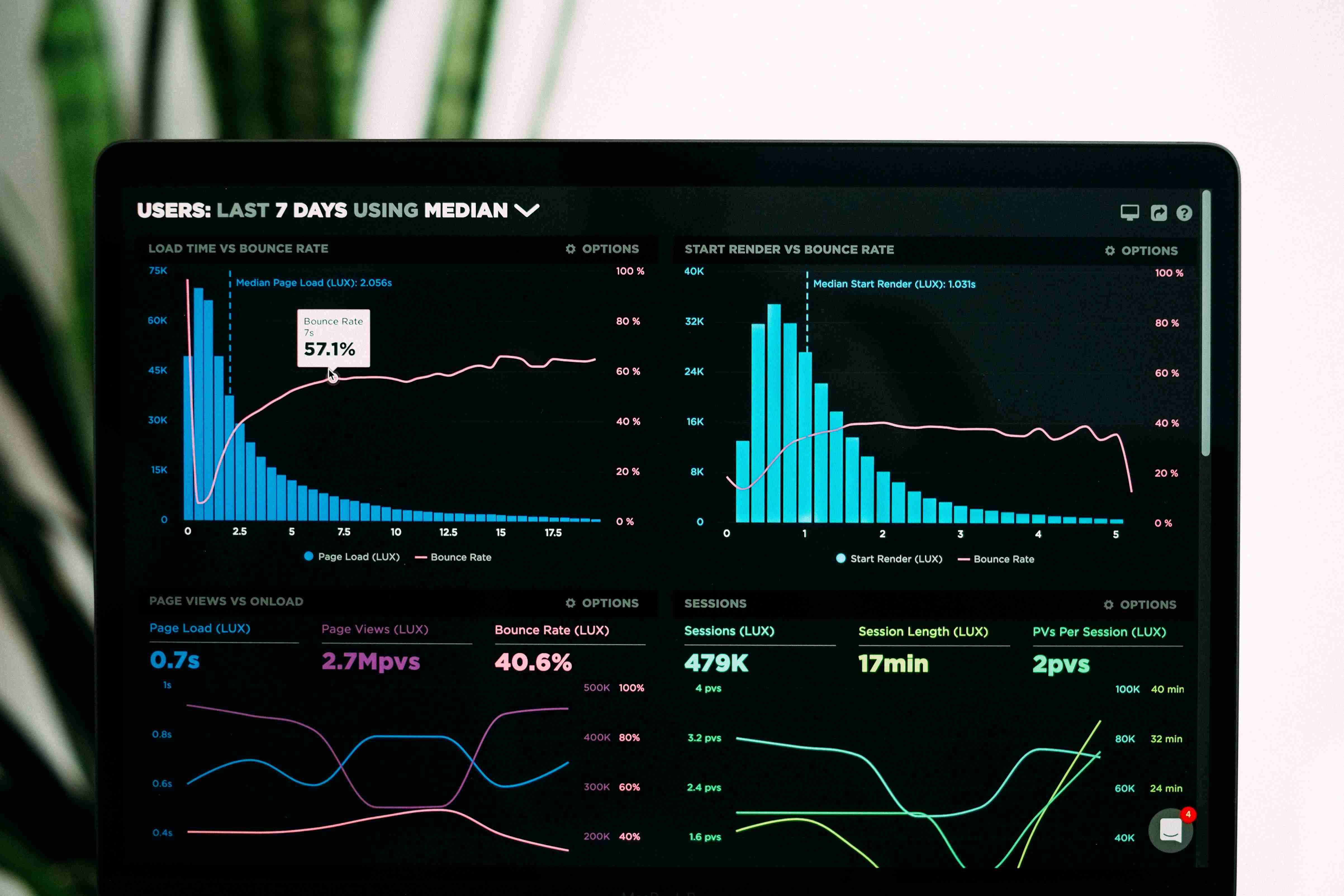
和黄医药三款肿瘤产品市场销售额
此前,信达生物PD-1肿瘤药和传奇生物CAR-T疗法闯关美国食品药品监督管理局(FDA)收获不同的结果,引发国内医药行业的讨论。
和黄医药的索凡替尼也在等待FDA的审批。2021年7月,和黄医药公告称,美国食品药品监督管理局(FDA)已受理索凡替尼用于治疗胰腺和胰腺外(非胰腺)神经内分泌瘤的新药上市申请。FDA就该新药上市申请拟定的处方药用户付费法案(PDUFA)目标审评日期为2022年4月30日。
在此次线上见面会上,苏慰国表示,4月30日已经不远,现在还剩下的一些工作是核查,完成了一部分核查,还有一部分核查在等待通知,主要是生产现场核查和临床核查。基于目前的审批工作进展以及索凡替尼本身可以为患者带来的获益,“我们还是非常有信心”。
和黄医药已经围绕索凡替尼建立美国商业化团队,为索凡替尼在2022年于美国的潜在获批作准备。苏慰国介绍,该团队目前已经有54个人到岗,计划大概在6月底会达到84人。
值得一提的是,和黄医药提到,由于旅行限制,造成美国FDA对其在中国的生产设施的部分监管检的延期。公司将与监管机构保持密切合作,并关注不断变化的疫情。对于当前欧洲紧张的国际局势对业务的影响,苏慰国向澎湃新闻记者表示,和黄医药在俄罗斯和乌克兰都没有任何的临床研究,目前没有影响。
在国内,和黄医药参与了2021年医保谈判,最终索凡替尼获首次纳入医保目录,较2021年标价降低52%;呋喹替尼较2021版目录降价5%获得续约;赛沃替尼参与了谈判,但并未成功进入医保目录。
医保降价是否会影响销售额?陈洪以索凡替尼为例分析称,今年一二月份,索凡替尼市场销售额比去年同期增长21%。公司对于市场销售金额的增长能够弥补掉降价幅度,是充满了信心的。
2011年,双方就赛沃替尼达成合作协议,和黄医药负责沃瑞沙在中国的临床开发、上市许可、生产和供应,阿斯利康负责其商业化。陈洪表示,在今年的医保谈判的时候,相信阿斯利康也会积极去跟政府沟通,来尽量争取赛沃替尼进入到国家医保。
校对:张亮亮

